Anne Gelderloos, Forscherin für Infektionskrankheiten am Zentrum für die Kontrolle von Infektionskrankheiten, Nationales Institut für öffentliche Gesundheit und Umwelt (RIVM), Bilthoven, Niederlande, Puck B. van Kasteren, Ph.D., ein Molekularvirologe am Netherlands Center for Immunology of Infectious Diseases and Vaccines, dem Zentrum, das die niederländische Regierung in Fragen der Immunologie und Vakzinologie berät, und Kollegen untersuchen die IgG-Subklassen-Antworten in einer alternden Bevölkerung nach einer mRNA-COVID-19-Impfung, um die Beziehung dieser Kohorte zur Fc-vermittelten Antikörper-Effektor-Funktionalität zu beurteilen.
Hintergrund
Es gibt immer mehr Hinweise darauf, dass eine wiederholte COVID-19-mRNA-Impfung einen signifikanten Anstieg der SARS-CoV-2-Spike-spezifischen Serumantikörper der IgG4-Subklasse auslöst. Nach Ansicht der Experten aus den Niederlanden deutet ein solches Phänomen auf einen „weitreichenden Wechsel der Immunglobulinklasse nach einer Auffrischungsimpfung“ hin.
Gibt es bereits Belege für einen Anstieg der IgG4-Antworten nach mehreren mRNA-Dosen? Ja. Es war jedoch unklar, ob dies auch bei gesunden älteren Erwachsenen (≥ 65 Jahre) der Fall ist.
Ergebnisse der Studie
Das Studienteam quantifizierte das Serum älterer Erwachsener (n= 38-50, 65-83 Jahre) einen Monat nach der zweiten, dritten und fünften Impfung, indem es die Konzentrationen der Spike-S1-spezifischen IgG-Subklassen (ausgedrückt in willkürlichen Einheiten pro ml), die antikörperabhängige NK-Zellaktivierung, die Komplementablagerung und die Monozyten-Phagozytose maß und dann die Subklassenverteilung im Serum mit derjenigen jüngerer Erwachsener (n= 64, 18-47 Jahre) einen Monat nach der zweiten und dritten Impfung verglich.
Gelderloos und Kollegen berichten in der von Experten begutachteten Fachzeitschrift Immunity & Aging:
„Im Vergleich zu jüngeren Personen wiesen ältere Erwachsene einen Monat nach der dritten Impfung erhöhte IgG2- und IgG4-Werte auf (was möglicherweise mit anderen Faktoren als dem Alter zusammenhängt) und einen weiteren Anstieg nach der fünften Impfung. Die Fähigkeit spezifischer Serumantikörper, die NK-Zellaktivierung und Komplementablagerung zu vermitteln, nahm im Verhältnis zu den S1-spezifischen Gesamt-IgG-Konzentrationen nach wiederholter Impfung ab. Dieser Rückgang ist mit einem erhöhten IgG4/IgG1-Verhältnis verbunden.
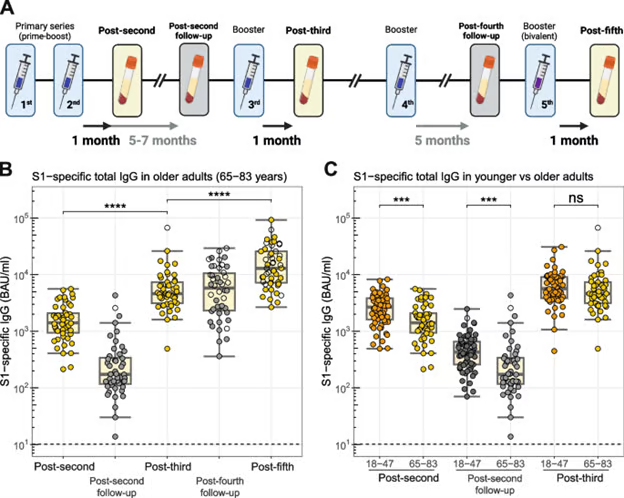
In der nachstehenden Grafik zeigt das Studienteam, dass eine wiederholte COVID-19-mRNA-Impfung bei älteren Erwachsenen zu einem Wechsel der IgG4-Klasse und einer geringeren NK-Zellaktivierung durch S1-spezifische Antikörper führt. Die Autoren geben unten eine Beschreibung.
SARS-CoV-2-Spike S1-spezifische Gesamt-IgG-Spiegel bei jüngeren und älteren Erwachsenen nach mRNA-Impfung. A Schematischer Überblick über das Impf- und Probenahmeschema, bei dem die Teilnehmer ursprünglich monovalente (1. bis 4. Dosis) und bivalente (5. Dosis) mRNA-Impfstoffe erhielten. Die SARS-CoV-2-Spike-S1-spezifischen Gesamt-IgG-Konzentrationen (BAU/ml) nach der mRNA-Impfung wurden im Serum mittels Multiplex-Immunoassay für B ältere Erwachsene (n = 50) bis zu einem Monat nach der fünften Impfung und für C jüngere (n = 64) und ältere (n = 50) Erwachsene bis zu etwa einem Monat nach der dritten Impfung gemessen. Die gestrichelten Linien zeigen den Cut-off-Wert für Seropositivität an. SARS-CoV-2-infizierte Personen (basierend auf N-Seropositivität) sind durch offene Kreise gekennzeichnet. Die Unterschiede zwischen den Gruppen wurden mit einem nichtparametrischen (ungepaarten) Wilcoxon Signed Rank Test mit Bonferroni-Korrektur für Mehrfachtests ermittelt. *** P < 0,001; **** P < 0,0001. BAU, bindende Antikörpereinheiten; N, Nukleoprotein; ns, nicht signifikant.
Die Autoren berichten über einen relativen Rückgang von ADNKA und ADCD, der bei wiederholter mRNA-Impfung bei älteren Erwachsenen beobachtet wird und mit einem Anstieg des Verhältnisses von IgG4/IgG1-Konzentration einhergeht.
Sie beschreiben Abbildung 6 als den Zusammenhang zwischen Fc-vermittelten Effektor-Funktionen und IgG4/IgG1-Verhältnissen oder IgG-Avidität bei älteren Erwachsenen. Die Fähigkeit von Spike-S1-spezifischen Serumantikörpern, ADNKA, ADCD und Monozyten-ADCP nach einer mRNA-Impfung bei älteren Erwachsenen (n = 38) etwa einen Monat nach der dritten und fünften Impfung zu vermitteln, im Verhältnis zu den S1-spezifischen Gesamt-IgG-Spiegeln zum gleichen Zeitpunkt. Farbskalen zeigen das IgG4/IgG1-Verhältnis (A) oder den Aviditätsindex (B) der SARS-CoV-2-Spike-S1-spezifischen Antikörper an. Die gepunkteten Linien zeigen den Wert der Negativkontrolle (Serumprobe vor der Pandemie) an. Die durchgezogenen grauen Linien wurden mittels linearer Regression (gerade Linien) oder lokaler Streudiagrammglättung (LOESS) erstellt. SARS-CoV-2-infizierte Personen (basierend auf N-Seropositivität) sind durch offene Kreise gekennzeichnet. ADCD, Antikörper-abhängige Komplementdeposition; ADCP, Antikörper-abhängige zelluläre Phagozytose; ADNKA, Antikörper-abhängige natürliche Killerzellaktivierung; BAU, bindende Antikörpereinheiten; iMFI, integrierte mittlere Fluoreszenzintensität; N, Nukleoprotein.
IgG4: Was sind die möglichen Indikationen?
Forschungsarbeiten haben gezeigt, dass der IgG4-Spiegel nach mehrfacher Verabreichung von mRNA-COVID-19-Impfstoffen (wie Pfizer-BioNTech und Moderna) ansteigen kann. IgG4 ist eine der vier Unterklassen von Immunglobulin G (IgG), einem Antikörper, der eine entscheidende Rolle bei der Immunantwort spielt. Er ist typischerweise an Toleranzmechanismen beteiligt und trägt dazu bei, Immunreaktionen zu modulieren, um übermäßige Entzündungen zu verhindern.
In einigen Studien, über die TrialSite berichtet, wurde nach der Verabreichung mehrerer mRNA-Impfstoffdosen (insbesondere Auffrischungsdosen) eine Verschiebung der Immunreaktion beobachtet, wobei ein größerer Anteil der gebildeten Antikörper zur IgG4-Unterklasse gehört. Diese Verschiebung der Subklassen könnte eine verfeinerte Immunantwort widerspiegeln, die darauf abzielt, eine überaktive Immunreaktion zu verhindern.
Daraus können sich einige Herausforderungen ergeben. IgG4 wird häufig mit Immuntoleranz in Verbindung gebracht, was bedeutet, dass es dem Immunsystem helfen kann, mit der Zeit weniger reaktiv zu sein. Diese Veränderung könnte mit einer längeren oder wiederholten Antigenexposition zusammenhängen, wie sie bei mehreren Impfstoffdosen auftritt.
Sind die Auswirkungen auf die Immunität? Ja. Zwar ist IgG4 im Allgemeinen weniger wirksam bei der Neutralisierung von Viren als andere IgG-Unterklassen (z. B. IgG1), doch könnte sein Anstieg auf eine langfristige, ausgewogene Immunreaktion hindeuten, die immer noch Schutz vor schweren Erkrankungen bieten kann, aber möglicherweise die Intensität der Entzündungsreaktion auf den Impfstoff verringert.
Insgesamt ist der Anstieg des IgG4-Spiegels nach einer mRNA-Impfung ein interessanter Aspekt der Anpassung des Immunsystems an wiederholte Impfstoffexpositionen, wenngleich weitere Forschungsarbeiten erforderlich sind, um seine klinische Bedeutung vollständig zu verstehen.
Der Anstieg der IgG4-Produktion nach mehreren Auffrischungsimpfungen mit dem mRNA-Impfstoff COVID-19 wirft interessante Fragen zur Immunantwort auf, doch die mit dieser Veränderung verbundenen Risiken werden noch untersucht. TrialSite gibt einen Überblick über einige Überlegungen zum Thema der erhöhten IgG4-Produktion.
Eine Verringerung der antiviralen Wirksamkeit könnte ein Problem darstellen. IgG1 und IgG3, die bei der Neutralisierung von Viren und der Aktivierung von Immunzellen effizienter sind, sind in der Regel die dominierenden Unterklassen, die als Reaktion auf Infektionen oder Impfstoffe gebildet werden.
IgG4 hingegen hat eine weniger entzündungsfördernde und neutralisierende Wirkung. Einige Forscher vermuten, dass ein erhöhter Anteil von IgG4 theoretisch die Gesamtwirksamkeit der Immunantwort gegen das Virus verringern könnte, insbesondere bei der Verhinderung einer Infektion. Dies könnte sich jedoch nicht wesentlich auf den Schutz vor schweren Erkrankungen auswirken.
Allerdings könnte die Immuntoleranz, wie oben beschrieben, ein Problem darstellen. IgG4 wird häufig mit Immuntoleranz und gedämpften Immunreaktionen in Verbindung gebracht, was zur Vermeidung übermäßiger Entzündungen oder Autoimmunreaktionen von Vorteil sein kann. Im Zusammenhang mit einer Virusinfektion könnte eine zu große Toleranz jedoch theoretisch die Fähigkeit des Immunsystems schwächen, das Virus zu bekämpfen.
Es besteht die Befürchtung, dass diese Verschiebung im Laufe der Zeit zu einer weniger robusten Immunreaktion führen könnte, obwohl dies im Zusammenhang mit COVID-19 nicht schlüssig nachgewiesen wurde.
Bei der Allergie-Immuntherapie wird die IgG4-Produktion gezielt angeregt, um allergische Reaktionen zu verringern. Einige Forscher haben Analogien zwischen diesem Prozess und der wiederholten Verabreichung von mRNA-Impfstoffen gezogen und vermuten, dass sich das Immunsystem in einen toleranteren Zustand versetzen könnte. Ob dies im Falle von Virusinfektionen vorteilhaft oder nachteilig ist, wird noch untersucht.
Was die laufende Forschung anbelangt, so deuten zwar einige Studien darauf hin, dass eine erhöhte IgG4-Produktion mit einer verfeinerten Immunantwort nach mehreren Impfstoffdosen einhergehen könnte, doch die klinischen Auswirkungen – ob positiv oder negativ – sind noch unklar. Wichtig ist, dass Impfstoffe nach wie vor einen starken Schutz vor schweren Erkrankungen und Tod bieten.
Steht IgG4 in Verbindung mit Krebs?
Problematisch ist, dass ein Anstieg der IgG4-Produktion mit bestimmten Krebsarten in Verbindung gebracht wird, obwohl die Beziehung komplex und kontextabhängig ist. In einigen Fällen sind erhöhte IgG4-Werte mit einem immunsuppressiven Umfeld verbunden, das das Tumorwachstum begünstigen könnte, während sie in anderen Fällen Teil der Immunreaktion des Körpers auf den Tumor sein können.
Trotz dieser potenziellen IgG4-Verschiebung haben sich mRNA-Impfstoffe als hochwirksam bei der Verhinderung schwerer Folgen von COVID-19 erwiesen, insbesondere im Zusammenhang mit mehreren Varianten, zumindest laut der Mehrheit der gängigen Literatur. Einige Wissenschaftler und Ärzte haben jedoch die Objektivität der umfangreichen Literatur zu diesem Thema in Frage gestellt. Das medizinische Establishment vertritt wahrscheinlich die Ansicht, dass das praktische Risiko im Zusammenhang mit dieser Antikörperverschiebung wahrscheinlich minimal ist, obwohl längerfristige Studien erforderlich sind, um die Auswirkungen vollständig zu verstehen.
Zum gegenwärtigen Zeitpunkt scheint der beobachtete Anstieg von IgG4 nach mehreren Auffrischungsimpfungen nicht auf erhebliche unmittelbare Risiken hinzuweisen, insbesondere was die Verhinderung schwerer Erkrankungen und Krankenhausaufenthalte betrifft. Es sind jedoch weitere Untersuchungen erforderlich, um festzustellen, ob diese Verschiebung langfristige Auswirkungen auf die Immunität oder den Schutz haben könnte.
Puck B. van Kasteren, PhD, Korrespondierender Autor
Finanzierung der Studie
Niederländisches Ministerium für Gesundheit, Wohlfahrt und Sport (VWS)
Forschungsleiter/Investigator
- Anne T. Gelderloos, MS, Zentrum für Immunologie von Infektionskrankheiten und Impfstoffen (IIV), Zentrum für die Kontrolle von Infektionskrankheiten, Nationales Institut für öffentliche Gesundheit und Umwelt (RIVM), Bilthoven, die Niederlande
- Marije K. Verheul, Zentrum für Immunologie von Infektionskrankheiten und Impfstoffen (IIV), Zentrum für die Bekämpfung von Infektionskrankheiten, Nationales Institut für Volksgesundheit und Umwelt (RIVM), Bilthoven
- Irene Middelhof, Zentrum für Immunologie von Infektionskrankheiten und Impfstoffen (IIV), Zentrum für die Bekämpfung von Infektionskrankheiten, Nationales Institut für Volksgesundheit und Umwelt (RIVM), Bilthoven
- Mary-Lène de Zeeuw-Brouwer,
- Robert S. van Binnendijk, Zentrum für Immunologie von Infektionskrankheiten und Impfstoffen (IIV), Zentrum für die Bekämpfung von Infektionskrankheiten, Nationales Institut für Volksgesundheit und Umwelt (RIVM), Bilthoven
- Anne-Marie Buisman, Zentrum für Immunologie von Infektionskrankheiten und Impfstoffen (IIV), Zentrum für die Bekämpfung von Infektionskrankheiten, Nationales Institut für Volksgesundheit und Umwelt (RIVM), Bilthoven
- Puck B. van Kasteren, PhD, Zentrum für Immunologie von Infektionskrankheiten und Impfstoffen (IIV), Zentrum für die Kontrolle von Infektionskrankheiten, Nationales Institut für Volksgesundheit und Umwelt (RIVM), Bilthoven; Korrespondierender Autor
Quelle: Zeitschrift Immunity & Aging
Schreibe einen Kommentar
Du musst angemeldet sein, um einen Kommentar abzugeben.